class 10 NCERT Science chapter-3 text book question and answer part-1 //Metals and Non-Metals
अध्याय-3
धातु एवं अधातु
प्रश्न-1. निम्न में कौनसा युगल विस्थापन अभिक्रिया प्रदर्शित करता है ।
अ) NaCl विलयन एवं कॉपर धातु
ब) MgCl2 विलयन एवं ऐल्युमिनियम धातु
स) FeSO4 विलयन एवं कॉपर धातु
द) AgNO3 विलयन एवं कॉपर धातु
उत्तर – द) AgNO3 विलयन एवं कॉपर धातु
स्पष्टीकरण –
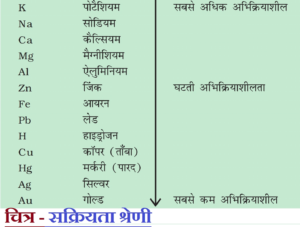
सक्रियता श्रेणी से स्पष्ट है कि AgNO3 विलयन एवं कॉपर धातु (Cu) के युगल में Cu , Ag(सिल्वर) से अधिक क्रियाशील है अतः यह AgNO3 के विलयन से अभिक्रिया कर Ag को विस्थापित कर देती है और स्वयं नाइट्रेट यौगिक बना लेती है । अभिक्रिया निम्न प्रकार होती है –
2AgNO3 + Cu → Cu(NO3)2 + 2Ag
प्रश्न-2. लौहे के फ्राइंग पैन (frying pen) को जंग से बचाने के लिए निम्न में से कौनसी विधि उपयुक्त है –
अ) ग्रीज लगाकर
ब) पेंट लगाकर
स) जिंक की परत चढ़ाकर
द) उपरोक्त सभी
उत्तर – द) उपरोक्त सभी
स्पष्टीकरण – उपरोक्त सभी विधियाँ लौहे को ऑक्सीजन और जल से अभिक्रिया करने से रोकती है जिससे लौहे से बनी वस्तु अधिक समय तक सुरक्षित रहती है और उस पर जंग नहीं लगती है ।
प्रश्न-3. कोई धातु ऑक्सीजन के साथ अभिक्रिया कर उच्च गलनांक वाला यौगिक निर्मित करती है । यह यौगिक जल में विलेय है । यह तत्व क्या हो सकता है –
अ) कैल्सियम
ब) कार्बन
स) सिलिकन
द) लोहा
उत्तर –अ) कैल्सियम
स्पष्टीकरण – कैल्सियम धातु ऑक्सीजन के साथ अभिक्रिया कर उच्च गलनांक वाला यौगिक बनाती है जो कि कैल्सियम ऑक्साइड (CaO) है । यह यौगिक जल में विलेय होता है । CaO को बिना बुझा हुआ चुना भी कहते है ।
प्रश्न-4. खाद्य पदार्थ के डिब्बों पर जिंक की बजाय टिन का लेप होता है क्योंकि –
अ) टिन की अपेक्षा जिंक महँगा है ।
ब) टिन की अपेक्षा जिंक का गलनांक अधिक है ।
स) टिन की अपेक्षा जिंक अधिक अभिक्रियाशील है ।
द) टिन की अपेक्षा जिंक कम अभिक्रियाशील है ।
उत्तर – स) टिन की अपेक्षा जिंक अधिक अभिक्रियाशील है ।
स्पष्टीकरण – जिंक , टिंन की अपेक्षा अधिक अभिक्रियाशील होता है । यदि हम टिंन धातु का उपयोग खाद्य पदार्थ के डिब्बों पर लेप चढ़ाने में करते है तो टिंन कम क्रियाशील होने के कारण वायुमण्डलीय कारकों से बहुत कम क्रिया करता है जिससे लंबे समय तक खाद्य पदार्थों को डिब्बों में सुरक्षित रखा जा सकता है । यदि टिंन की बजाय जिंक का उपयोग किया जाए तो खाद्य पदार्थों को लंबे समय तक सुरक्षित नहीं रखा जा सकता है क्योंकि जिंक , टिंन से अधिक अभिक्रियाशील होता है ।
प्रश्न-5. आपको एक हथोड़ी ,बैटरी, बल्ब, तार एवं स्विच दिया गया है –
(a) इनका उपयोग कर धातुओं एवं अधातुओं के नमूनों के बीच आप विभेद कैसे कर सकते है ।
(b) धातुओं एवं अधातुओं में विभेदन के लिए इन परीक्षणों की उपयोगिताओं का आकलन कीजिए ।
उत्तर- (a) (i) हथोड़े की चोट से यदि दिया गया नमूना टूट जाता है ,तो वह अधातु है । परन्तु यदि वह पतली चादर के रूप में परिवर्तित हो जाता है ,तो वह धातु है क्योंकि धातु आघातवर्ध्य होती है ।
(ii) दिए गए उपकरणों (बैटरी, बल्ब, तार एवं स्विच) को जोड़कर एक परिपथ तैयार करते हैं और इसके दोनों टर्मिनलों के बीच नमूनों को रखते हैं । स्विच ऑन करने पर यदि बल्ब जलता है ,तो नमूना धातु है क्योंकि धातुएँ विद्युत की सुचालक होती है और यदि बल्ब नहीं जलता है तो नमूना अधातु है ।
(b) धातुओं एवं अधातुओं में विभेदन के लिए इन परीक्षणों की उपयोगिताओं का आकलन- इन परीक्षणों के आधार के आधार पर हम बता सकते है कि
(i) धातुएँ आघातवर्धनीय होती हैं अतः इनकी चादर बनाकर विभिन्न प्रकार के बर्तन ,पात्र व विभिन्न वस्तुएँ बनाई जाती है जबकि अधातुओं में ऐसा नहीं हो सकता ।
(ii) धातुएँ विद्युत की सुचालक होती है ,अतः इनसे विद्युत के तार आदि बनाए जाते हैं । जबकि अधातुओं में ऐसा नहीं हो सकता ।
प्रश्न-6. उभयधर्मी ऑक्साइड क्या होते है । दो उभयधर्मी ऑक्साइडों का उदाहरण दीजिए तथा उभयधर्मी ऑक्साइड की अम्ल व क्षार के साथ अभिक्रिया भी लिखिए ।
उत्तर- उभयधर्मी ऑक्साइड – ऐसे ऑक्साइड जो अम्ल तथा क्षारक दोनों से अभिक्रिया करके लवण तथा जल बनाते हैं, उन्हें उभयधर्मी ऑक्साइड कहते है ।
उदाहरण –ऐलुमिनियम ऑक्साइड (Al2O3) एवं जिंक ऑक्साइड (ZnO)
अम्ल तथा क्षारक के साथ उभयधर्मी ऑक्साइड (ऐलुमिनियम ऑक्साइड) निम्न प्रकार से अभिक्रिया करता है –
Al2O3 + 6HCl → 2AlCl3 + 3H2O
उपरोक्त अभिक्रिया में उभयधर्मी ऑक्साइड क्षारीय व्यवहार प्रदर्शित करता है ।
Al2O3 + 2NaOH → 2NaAlO2 (सोडियम ऐलुमिनेट) + H2O
उपरोक्त अभिक्रिया में उभयधर्मी ऑक्साइड अम्लीय व्यवहार प्रदर्शित करता है ।
प्रश्न-7. दो धातुओं के नाम बताइए जो तनु अम्ल से हाइड्रोजन को विस्थापित कर देंगे तथा दो धातुएँ जो ऐसा नहीं कर सकती हैं ।
उत्तर- Mg तथा Zn तनु अम्लों के साथ क्रिया करके हाइड्रोजन को विस्थापित करते हैं जबकि Cu तथा Ag ऐसा नहीं करते है क्योंकि Mg तथा Zn हाइड्रोजन से अधिक क्रियाशील हैं जबकि Cu तथा Ag कम क्रियाशील हैं ।
प्रश्न-8. किसी धातु M के विद्युत अपघटनी परिष्करण में आप ऐनोड, कैथोड एवं विद्युत अपघट्य कैसे बनाएंगे ।
उत्तर- किसी धातु M के विद्युत अपघटनी परिष्करण में अशुद्ध धातु को ऐनोड तथा शुद्ध धातु की पतली परत को कैथोड बनाया जाता है । धातु के लवण के विलयन का उपयोग विद्युत अपघट्य के रूप में किया जाता है । जैसे Cu (कॉपर) धातु के शोधन में CuSO4 का विलयन विद्युत अपघट्य के रूप में किया जाता है ।



