क्लास-10 अध्याय-3 धातु एवं अधातु #class 10 ncert science chapter-3 part-2
3. धातु की अम्ल के साथ अभिक्रिया
धातु की अम्ल के साथ अभिक्रिया कराने पर धातु लवण व हाइड्रोजन गैस बनती है ।
उदाहरण-
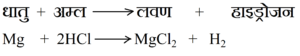
4. धातु की अन्य धातु के लवण के साथ अभिक्रिया
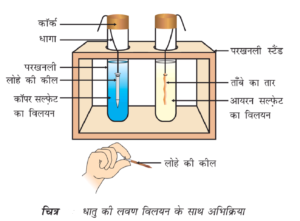
धातु की अभिक्रिया जब अन्य धातु के लवण के साथ कराते है तो सक्रियता श्रेणी में उपस्थित धातुएं ,अपने से नीचे स्थित धातुओं के लवण में से धातु को प्रतिस्थापित कर देती है और स्वयं अपना लवण बना लेती है ।
उदाहरण- जब कॉपर सल्फेट के नीले विलयन में लोहे (आयरन)की कील डालते है तो कॉपर सल्फेट का नीला रंग विलुप्त हो जाता है ,क्योंकि आयरन के परमाणु, कॉपर की जगह ले लेते है और आयरन सल्फेट का लवण बन जाता है ।
![]()
⦁ ऐक्वा रेजिया (रॉयल जल) – जब सांद्र हाइड्रोक्लोरिक अम्ल (HCl ) तथा सांद्र नाइट्रिक अम्ल (HNO3 ) को 3:1 में मिश्रित करते है तो ऐक्वा रेजिया का निर्माण होता है । यह गोल्ड को गला सकता है ।
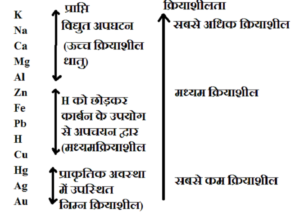
⦁ सक्रियता श्रेणी- वह श्रेणी जिसमें तत्वों को उनकी क्रियाशीलता के आधार पर व्यवस्थित किया जाता है ,उसे सक्रियता श्रेणी कहते है ।
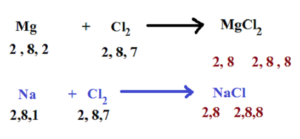
⦁ आयनिक यौगिक या वैद्युत संयोजक यौगिक –
धातु से अधातु में e- के स्थानान्तरण से बने यौगिकों को आयनिक यौगिक या वैद्युत संयोजक यौगिक कहते है । उदा.
⦁ खनिज –
पृथ्वी की भूपर्पटी में प्राकृतिक रूप से पाए जाने वाले तत्वों या यौगिकों को खनिज कहते है ।
⦁ अयस्क-
ऐसे खनिज जिसमें कोई धातु काफी मात्रा में होती है और जिसे निकालना लाभकारी होता है उन्हें अयस्क कहते है ।
⦁ गोल्ड (Au), सिल्वर (Ag), प्लेटिनम (Pt) एंव कॉपर (Cu) प्रकृति में स्वतंत्र अवस्था में पाए जाते है ।
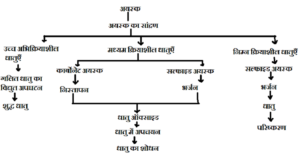
⦁ धातुओं का निष्कर्षण-
⦁ गैंग – पृथ्वी से प्राप्त अयस्कों में मिट्टी, रेत , आदि जैसी अशुद्धियाँ होती
है जिन्हें गैंग कहते है ।
⦁ जंग – लंबे समय तक आर्द्र वायु में रहने पर लोहे पर भूरे रंग की पतली परत चढ़ जाती है जिसे जंग कहते है । इससे धातु संक्षारित होने लगती है , इस प्रक्रिया को ही संक्षारण कहते है ।
संक्षारण से सुरक्षा के उपाय-
पेंट करके, तेल लगाकर, ग्रीज लगाकर, यशदलेपन द्वारा, क्रोमियम लेपन द्वारा, ऐनोडीकरण द्वारा, या मिश्र धातु बनाकर लोहे को जंग लगने से बचाया जा सकता है ।
⦁ यशदलेपन –
लोहे एंव इस्पात (स्टील) को जंग से सुरक्षित रखने के लिए उन पर जस्ते (जिंक) की पतली परत चढ़ाने की विधि को यशदलेपन कहते है ।
⦁ लोहे के साथ निकैल एंव क्रोमियम मिलाने पर हमें स्टेनलेस स्टील(इस्पात) प्राप्त होता है , जो कठोर होता है और उसमें जंग नहीं लगती है ।
⦁ मिश्रातु/मिश्रधातु –
दो या दो से अधिक धातुओं के समांगी मिश्रण को मिश्रातु/मिश्रधातु कहते है । उदा.
पीतल (Zn व Cu ), काँसा (Sn व Cu )
⦁ इलेक्ट्रॉन बिन्दू संरचना –
तत्व के बाह्यत्तम कोश में उपस्थित इलेक्ट्रॉनों को बिन्दू के रूप में तत्व के चारों ओर प्रदर्शित करना इलेक्ट्रॉन बिन्दू संरचना कहलाता है । उदा.
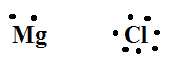
⦁ धातुएँ व अधातुओं की क्रिया-
धातुएँ इलेक्ट्रॉन त्यागकर व अधातुएँ इलेक्ट्रॉन ग्रहण करके आपस में अभिक्रिया करती है जिससे उनके संयोजकता कोश पूर्ण हो जाते है और एक स्थायी यौगिक निर्मित होता है । उदा.

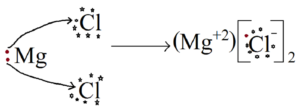
Very nice
Excellent read, I just passed this onto a colleague who was doing some research on that. And he just bought me lunch as I found it for him smile So let me rephrase that: Thanks for lunch! “The future is not something we enter. The future is something we create.” by Leonard I. Sweet.